Les résultats d’une étude menée par des scientifiques du Luxembourg centre for systems biomedicine de l’Université du Luxembourg (LCSB), du Luxembourg institute of health (LIH) et du Laboratoire national de santé (LNS), réalisée en collaboration avec des chercheurs japonais, pourraient bien changer la donne pour la maladie de Parkinson, mais aussi pour la démence à corps de Lewy et l’atrophie multi-systématisée. Des pathologies qui font toutes partie du groupe des maladies neurodégénératives appelées synucléinopathies.
Pouvoir diagnostiquer la maladie de Parkinson à l’aide d’une simple prise de sang constituera un progrès majeur.
Les chercheurs ont en effet identifié un biomarqueur véhiculé par le sang pouvant refléter la propagation de la maladie de Parkinson. Grâce à la méthode IP/RT-QuIC – développée par l’équipe du professeur Nobutaka Hattori du département de neurologie de l’Université de Juntendo et directeur du Neurodegenerative disorders collaboration laboratory au RIKEN Centre for brain science – les scientifiques ont pu détecter des fibrilles d’α-synucléine dans le sérum de 95% des patients atteints de synucléinopathies. Cette découverte représente une avancée importante vers la mise au point d’un test diagnostic basé sur une prise de sang.
«Pouvoir diagnostiquer la maladie de Parkinson à l’aide d’une simple prise de sang constituera un progrès majeur, car actuellement cela repose en grande partie sur un examen clinique effectué par un neurologue», souligne le professeur Rejko Krüger, directeur du département transversal translational medicine au LIH et responsable de l’équipe transnationale neuroscience au LCSB.
Une banque de cerveaux au Luxembourg
Pour arriver à ces résultats, les chercheurs luxembourgeois et japonais ont suivi «plus de 900 personnes ayant la maladie de Parkinson et d’autres formes de parkinsonisme depuis neuf ans. Grâce à des visites annuelles, nous pouvons retracer l’évolution clinique de ces patients. Nous avons de plus collecté des échantillons de sang et de liquide céphalo-rachidien, ainsi que de tissu cérébral lors d’autopsies», détaillent-ils.

Les professeurs Rejko Krüger et Nobutaka Hattori ont collaboré dans la recherche qui a permis de faire une découverte majeure pour diagnostiquer des maladies neurodégénératives. (Photo: Université du Luxembourg)
«Nous avons également créé une banque de cerveaux au Luxembourg, ce qui nous donne accès aux cerveaux légués par certains patients pour des analyses post-mortem. Cela fournit des données neuropathologiques complémentaires, la référence pour le diagnostic des maladies neurodégénératives, qui permettent de valider les observations cliniques», ajoute le professeur Michel Mittelbronn, directeur du LNS.
La découverte va même encore plus loin, car les scientifiques ont montré que la structure et les propriétés des fibrilles d’α-synucléine différaient en fonction de chaque synucléinopathie dont peut être atteint le patient. En plus de servir au diagnostic de la maladie de Parkinson, ce marqueur pourrait donc permettre de distinguer plusieurs troubles neurodégénératifs entre eux.
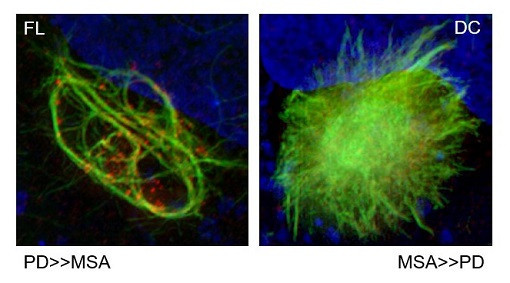
Images microscopiques en haute résolution de cultures cellulaires où l’alpha-synucléine (en vert) présente une structure filamenteuse (à gauche), plus susceptible de mener à la maladie de Parkinson, ou une structure à noyau dense (à droite), plus susceptible de mener à une atrophie multi-systématisée. (Visuel: Ayami Okuzumi)
«Nous sommes très fiers de contribuer à ces travaux de recherche grâce au Centre national d’excellence pour la recherche sur la maladie de Parkinson. Cela illustre l’importance du suivi à long terme de larges cohortes de patients. C’est en collectant ainsi des données exhaustives que nous pourrons de mieux en mieux répondre aux besoins des personnes atteintes de la maladie de Parkinson», conclut le professeur Rejko Krüger.
En 2022, ce dernier avait remporté, avec Ibrahim Boussaad, le prix du «Outstanding scientific achievement» lors des FNR Awards organisés par le Luxembourg national research fund (FNR) pour avoir réussi à développer la première preuve de concept pour la médecine de précision dans le domaine des maladies neurodégénératives.

